کاتالیزور از دو صفت کاتا و لیزور تشکیل شده است در زبان یونانی کاتا به معنای پائین، افتادن، یا پائین افتادن است و لیزور به معنی قطعه قطعه کردن میباشد. در برخی زبانها کاتالیزور را به معنی گردهم آوردن اجسام دور از هم معرفی کرده اند تجربه نشان داده است که واکنش با کاتالیزور در دمای کمتری صورت میگیرد و هم چنین کاتالیزور انرژی اکتیواسیون را کاهش میدهد یا باعث میشود ملکولهای درشت به ملکولهای کوچکتر قطعه قطعه و شکسته شوند.
این را هم بخوانید : نقش کاتالیست اگزوز در کاهش آلودگی هوا
اولین گزارش مربوط به کریشف می باشد که با استفاده از یک اسید به عنوان کاتالیزور توانست نشاسته را به قند هیدرولیزه کند. بعدها دیوی توانست واکنش اکسید اسیون هیدروژن را با اکسیژن در حضور کاتالیزور پلاتین انجام دهد که این واکنش یک واکنش گرماگیر بوده و در نتیجه هنگام انجام واکنش جرقه تولید میشد.
کاتالیزور به دو نوع کاتالیزور مرغوب و نامرغوب تقسیم میشود
کاتالیزور مرغوب به کاتالیزوری گفته می شود که فقط اجازه تشکیل یک نوع محصول را بدهد اگر در حضور کاتالیزور محصولات متفاوتی امکان تشکیل داشته باشند کاتالیزور نامرغوب تلقی میشود.
اولین کار در توضیح اینکه چرا یک واکنش کاتالیزوری انجام میگیرد و کاتالیزور چه نقشی دارد توسط فارادی انجام شد بیشترین بهرهبرداری از کاتالیزور در جنگ جهانی بود. دهه 1960 ـ 1950 دهه هایی است که با تولید کاتالیزورهای زیگرناتا ترکیبات بسیار هم و استراتژیک ساخته شد.
تاریخچه کشف کاتالیزورهای زیگلر-ناتا
 کاتالیزورهای زیگلر-ناتا به عنوان یک دسته مهم از کاتالیزورهای صنعتی نقش به سزایی در تولید پلیاولفینها دارند. اولین بار هولز کمپ دانشجوی محقق آلمانی، کارل زیگلر، کاملاً اتفاقی کاتالیزورهای زیگلر- ناتا را در انستیتو «ماکس پلانک» آلمان کشف کرد. وی فهمید اتیلن در مجاورت ترکیبات آلومنیوم و ترکیبات کلوئیدی نیکل، که به صورت کاملاً اتفاقی در راکتور بجا مانده بودند، در دمای پایین پلیمریزه میشود. همچنین ناتا و همکارانش نشان دادند که میتوان با کمک این دسته از کاتالیزورها پروپیلن را به صورت منظم فضایی پلیمریزه کرد. تا قبل از آن تهیه پلی پروپیلن با وزن مولکولی بالا تقریباً غیر ممکن بود و تنها پلی پروپیلن اتاکتیک با وزن مولکولی پایین تهیه میشد. کشف مذکور که به تهیه نوع خاصی از کاتالیزورها برای تهیه پلیاولفینها منجر شد چنان مهم بود که کارل زیگلر و جولیا ناتای ایتالیایی در سال 1956 برنده جایزه نوبل شیمی شدند. کشف کاتالیزورهای زیگلر- ناتا مسیر تحقیقات در زمینه پلیاولفینها را تغییر داد و با تغییراتی نه چندان بنیادی در این دسته از کاتالیزورها تولید پلیاولفینی با خواص مطلوب ممکن شد.
کاتالیزورهای زیگلر-ناتا به عنوان یک دسته مهم از کاتالیزورهای صنعتی نقش به سزایی در تولید پلیاولفینها دارند. اولین بار هولز کمپ دانشجوی محقق آلمانی، کارل زیگلر، کاملاً اتفاقی کاتالیزورهای زیگلر- ناتا را در انستیتو «ماکس پلانک» آلمان کشف کرد. وی فهمید اتیلن در مجاورت ترکیبات آلومنیوم و ترکیبات کلوئیدی نیکل، که به صورت کاملاً اتفاقی در راکتور بجا مانده بودند، در دمای پایین پلیمریزه میشود. همچنین ناتا و همکارانش نشان دادند که میتوان با کمک این دسته از کاتالیزورها پروپیلن را به صورت منظم فضایی پلیمریزه کرد. تا قبل از آن تهیه پلی پروپیلن با وزن مولکولی بالا تقریباً غیر ممکن بود و تنها پلی پروپیلن اتاکتیک با وزن مولکولی پایین تهیه میشد. کشف مذکور که به تهیه نوع خاصی از کاتالیزورها برای تهیه پلیاولفینها منجر شد چنان مهم بود که کارل زیگلر و جولیا ناتای ایتالیایی در سال 1956 برنده جایزه نوبل شیمی شدند. کشف کاتالیزورهای زیگلر- ناتا مسیر تحقیقات در زمینه پلیاولفینها را تغییر داد و با تغییراتی نه چندان بنیادی در این دسته از کاتالیزورها تولید پلیاولفینی با خواص مطلوب ممکن شد.
امروزه به جرأت میتوان گفت که تولید پلیمرها با اسـتفاده از کاتالیـزورهای زیگلر-ناتا یکی از مهمترین روشهاست و بیشترین سهم را در تولید پلیمرها دارد. در حال حاضر و با آن که نسل هشتم این کاتالیزورها در حال تشکیل است، هنوز کاتالیزورهای زیگلر-ناتا مهمترین عوامل تولید پلیاولفینها هستند و با گذشت حدود چهار دهه از عمر کاتالیزورهای متالوسن، که در برخی حالات تقریباً شبیه کاتالیزورهای زیگلر-ناتا هستند و با توجه به همین شباهتها برخی از محققان آنها را یکی از نسلهای کاتالیزورهای زیگلر-ناتا به حساب میآورند، هنوز در حدود 90 درصد از پلیاولفینها از روش کاتالیزورهای زیگلر-ناتا تهیه میشوند و کاتالیزورهای متالوسنی هنوز به صورت صنعتی نتوانستهاند جایگاهی مناسب بیابند و تنها چند شرکت، از جمله بازل، بصورت محدود پلیاولفینها را با کاتالیزورهای متالوسنی تولید کردهاند. در حال حاضر نسلهای جدید کاتالیزورهای زیگلر-ناتا فعالیت بسیار بالا و طول عمر کوتاهی دارند. کاتالیزورهای نسل اول بعضی مواقع تا 24 ساعت همچنان فعالیت خود را حفظ میکردند و به علت فعالیت کم و نسبت بالای کاتالیزور در محصول نهایی صنعتگران مجبور به شتشوی محصول و خنثی کردن کاتالیزور بودند، ولی امروزه با توجه به فعالیتهای بالای کاتالیزور، مقدار کاتالیزور آنقدر در محصول نهایی پایین است که مشکل شتشو و خنثی کردن کاتالیزور چندان وجود ندارد و همین باعث کاهش هزینههای تولید نیز شده است. بخشی دیگر از فعالیتهای محققان نیز در زمینه کاتالیزورهای زیگلر-ناتا در زمینه فضاگزینی است. کاتالیستهای زیگلر-ناتا میتوانند همگن و یا ناهمگن باشند ولی عمدتاً ناهمگن هستند و نوع محلول آنها به دلیل عدم پایداری کاتالیزور و کنترل نامناسب نظم فضایی معمولاً در صنعت استفاده نمیشوند. برای رفع این نقص کاتالیزورهایی بر پایه متالوسن در حال شکلگیری هستند. این کاتالیزورها محلولاند و میتوانند با آلومینواکسانها و دیگر کمک کاتالیزورها پلیاولفینها را با کنترل نظم فضایی؛ ریز ساختار عالی و توزیع وزن مولکولی باریک (به دلیل داشتن تنها یک نوع مرکز فعال) تولید کنند اما به علت مشکلات فرآیندی و صنعتی، پلیاولفینهایی که با این دسته از کاتالیزورها تولید میشوند هنوز از چند درصد کل پلیمرها تجاوز نکرده است. کاتالیستهای متالوسن برای کاربردهای اکستروژن و قالبگیری دمشی مناسب نیستند و فقط برای کاربردهای قالبگیری تزریقی مناسب هستند.
کاتالیزورهای زیگلر-ناتا
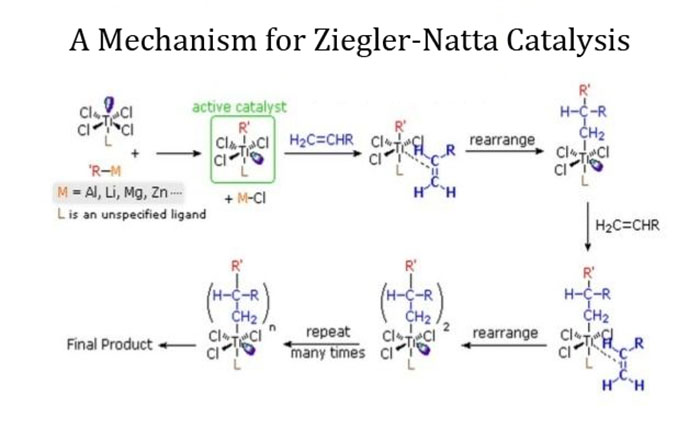 در کلیترین حالت کاتالیستهای زیگلر-ناتا از واکنش ترکیبات فلزات واسطه (بیشتر هالیدها) گروههای چهار تا هشت جدول تناوبی نظیر تیتانیوم، وانادیوم، کرمیوم، زیرکونیوم و… با آلکیل، آریل یا هالیدهای عناصر گروه یک تا چهار بوجود میآیند:
در کلیترین حالت کاتالیستهای زیگلر-ناتا از واکنش ترکیبات فلزات واسطه (بیشتر هالیدها) گروههای چهار تا هشت جدول تناوبی نظیر تیتانیوم، وانادیوم، کرمیوم، زیرکونیوم و… با آلکیل، آریل یا هالیدهای عناصر گروه یک تا چهار بوجود میآیند:
کاتالیست زیگلر-ناتای فعال هالید آلکیل یا آریل فلز + ترکیب فلز واسطه از گروه 1 تا 4 از گروه 4 تا 8
تعریف فوق کلی است و خیلی از ترکیبات بدست آمده، کاتالیستهای فعال نیستند. واکنش فوق در حلالهای آلی صورت میگیرد و در گزارش یک سیستم کاتالیستی زیگلر-ناتا نوع حلال نباید فراموش شود و پلیمریزاسیون اولفینها نیز با استفاده از حلالهای خنثی مثل هگزان، هپتان، تولوئن و…. انجام میشود. استفاده از حلالهای قطبی اثرات زیادی بر مکانسیم واکنش دارد. از جمله نکات دیگر این است که اگر کاتالیزور در محیط واکنش حل شود، سیستم پلیمریزاسیون را همگن و در غیر این صورت ناهمگن مینامند. ترکیبات آلی یا معدنی برای مقاصد خاص به این ترکیب دوتایی اولیه اضافه میشوند؛ برای مثال الکترون دهندهها برای بهبود ایزوتاکتیسیتی؛ نگهدارنده برای افزایش فعالیت کاتالیزور و هیدروژن برای کنترل وزن مولکولی. شباهت اجزای کاتالیزور زیگلر-ناتا در این است که یک موضع کئوردیناسیون خالی روی فلز واسطه وجود دارد و یک مولکول مونومر میتواند به آن متصل شود؛ دومین مولکول مونومر خود را به موضع کئوردیناسیون خالی بعدی متصل میکند که از آنجا میتواند با اولین مولکول متصل شده واکنش دهد. این سبب میشود که دومین موضع کئوردیناسیون دوباره خالی و امکان ورود مولکولهای بعدی مونومر و واکنش آنها با زنجیر پلیمر در حال رشد فراهم شود، به دلیل وضعیت فضایی خاص موجود در ترکیبات کئوردیناسیون فلزات واسطه، این نوع پلیمریزاسیون به صورت بسیار فضاویژه ادامه مییابد و پلیمری ایجاد میشود که در آن سر واحدهای مونومر ساختار شیمیایی مشابهی دارند؛ یعنی یک پلیمر ایزوتاکتیک به دست میآید.
ساختمان کاتالیزورهای زیگلر-ناتا
کاتالیزورها، هالیدهای فلزات واسطه گروههای چهار تا هشت جدول تناوبی و معروفترین و پرمصرفترین آنها TiCl3 و TiCl4 هستند. TiCl3 با غلتک به ذرات ریز فعال تبدیل میشود. محصول بدست آمده ساختمان بسیار منظم بلوری و چهار نوع ساختار بلوری ، و دارد که نوع بهترین نوع شناخته شده است. TiCl3 یک بلور یونی مانند سدیم کلراید و نسبتاً غیر متخلخل و با سطح ویژه کم (10-40 متر مربع بر گرم) است. همچنین نقطه ذوب بالایی دارد و در دمای 450 درجه سانتیگراد به TiCl4 و در دمای 830 درجه سانتیگراد به بخار TiCl4 تبدیل میشود.

دیدگاهتان را بنویسید